Cho 11,2 gam sắt \((\mathrm{Fe})\) tác dụng vừa đủ với dung dịch axit sunfuric \(\mathrm{H}_{2} \mathrm{SO}_{4} 10 \%\) thu được sắt (II) sunfat \(\left(\mathrm{FeSO}_{4}\right)\) và giải phóng khí hiđro \(\left(\mathrm{H}_{2}\right)\)
a) Tính thể tích khí tạo thành ở điều kiện tiêu chuẩn.
Giải thích:
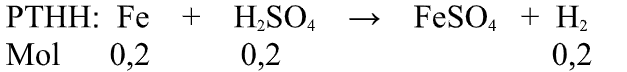
Số mol có trong 11,2 gam sắt.
\(\mathrm{n}_{\mathrm{Fe}}=\frac{m}{M}=\frac{11,2}{56}=0,4(\mathrm{~mol})\)Theo PTHH, số mol của \(\mathrm{H}_{2}\) là: \(\mathrm{n}_{\mathrm{H}_{2}}=\frac{0,2.1}{1}=0,2\) (mol)
Thể tích của 0,2 mol khí hiđro tạo thành ở đktc là:
\(\mathrm{V}_{\mathrm{H} 2}=\mathrm{n} .22,4=0,2 \cdot 22,4=4,48 \text { (1) }\)Câu hỏi này nằm trong: